
11. Februar 2020
Biologika – Möglichkeiten und Grenzen
Die biotechnologisch entwickelten Medikamente, kurz "Biologika", revolutionierten die Therapiekonzepte chronischer Erkrankungen. Für eine erfolgreiche Therapie sind aber nicht Rheumatologen allein verantwortlich, sondern es bedarf einer interdisziplinären Zusammenarbeit, da viele Patienten nicht nur an "einer" Krankheit leiden.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf allgemeineplus.at und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. universimed.com & med-Diplom.at)
… wie alles begann:
Am Anfang vor mittlerweile mehr als zwei Jahrzehnten standen beispielsweise die Erythropoetine, dann folgten die Biologika. Schlussendlich gipfelte die Entwicklung in den neuen Immuncheckpoint-Inhibitoren und in der Auszeichnung mit dem Nobelpreis im Jahre 2018 (James P. Allison und Tasuku Honjo). Doch das ist erst der Anfang einer weiteren bahnbrechenden Entwicklung. War es in den ersten Jahren noch von keiner großen Bedeutung, welche Erkrankungsmanifestation vorlag, so kann mittlerweile von einem individualisierten Vorgehen gesprochen werden, bei dem auf unterschiedliche Ausprägungen (Phänotypen) Rücksicht genommen werden kann. Zudem können auch Wünsche des Patienten berücksichtigt werden, was bei langjährigen Behandlungszyklen nicht unerheblich ist. Für eine erfolgreiche Therapie bedarf es allerdings einer interdisziplinären Zusammenarbeit, da viele Patienten nicht ausschließlich an "einer" Krankheit leiden.
… dann kam der Erfolg!
20 Jahre erfolgreicher Einsatz von TNF-Inhibitoren sind vielversprechend! Sie bieten ein gutes, sicheres Wirkprofil, keine erhöhte Karzinominzidenz, eine Senkung des kardiovaskulären Risikos etc. Auch sind bereits Biosimilars der effektiven Medikamente am Markt, was maßgeblich zu einer Kostensenkung beitrug (Kosten: 16000 Euro/Jahr).
Die Differenzierung der Behandlungsoptionen und die Kenntnis von Unterschieden der einzelnen Inhibitoren wie IL-6, IL-17, IL-23 etc. gegenüber den TNF-alfa-Inhibitoren und den Kinaseinhibitoren (JAK) sind vielfältig. Dies wird an einem kleinen Beispiel deutlich: So wirken zum Beispiel die IL-17-Inhibitoren effektiver an der Haut (Psoriasis) als die TNF-Inhibitoren, aber gleich gut an den Gelenken, dafür zeigen IL-17-Inhibitoren kein Ansprechen bei chronisch-entzündlichen Darmerkrankungen (CED). IL-23-Inhibitoren wirken hervorragend an der Haut (Psoriasis) und bei CED, hingegen geringer an den Gelenken und überhaupt nicht an der Wirbelsäule (Spondyloarthropathien).
Die Checkpoint-Inhibitoren im Rahmen der onkologischen Therapie ergänzen das Puzzle um einen weiteren essenziellen Teil: Die Erfolge dieser Therapiemöglichkeiten werden an der Überlebenszeit gemessen und diese ist nunmehr deutlich länger. Sogar Karzinome, die metastasiert sind, bleiben kontrollierbar. Melanome, Lungenkarzinome, Urothelkarzinome sowie Lymphome können in Zukunft immunologisch so blockiert werden, dass das eigene Immunsystem wieder die Kontrolle übernimmt. Die Onkologen fangen schon an in Jahren zu rechnen …! (Abb. 1)
Auszug aus der Literatur: "Lungenkarzinom – Überleben nicht vorbehandelter Patienten 29,6% nach 5 Jahren; bei vorbehandelten Patienten betrugen die entsprechenden 5-Jahres-Überlebensraten 25%. 3 von 4 dieser Patienten überlebten auch die 5-Jahresmarke."
Nach einer langen Zeit der alternativlosen (Er-)Duldung hat sich somit nicht nur in der Rheumatologie der Fokus deutlich verschoben: weg von einer abwartenden Haltung wegen der mitunter schwer toxischen Medikamente hin zu extrem wirkungsvollen, zielgerichteten Therapien.
Doch war da nicht noch etwas?
… woher stammt eigentlich diese Skepsis?
Bis in die 50er- und 60er-Jahre bedeutete eine Polyarthritis qualvolle weitere Lebensabschnitte. Der Tod trat mitunter entweder durch die Krankheit oder durch den Arzt (Therapieversuche) ein. 1950 erhielten Hensch, Reichenstein und Kendall den Nobelpreis für die Erforschung des Kortisons. Auf den ungezügelten Einsatz dieses damals weltweit für Furore sorgenden Medikaments folgte aber rasch eine gewisse Ernüchterung, als die massiven Nebenwirkungen zutage traten. Auch die modernen Biologika sind nicht ohne Nebenwirkungen, wobei jedoch anzumerken ist, dass vorwiegend die Zell-Zell-Interaktionen, also nur die Zytokine, beeinflusst werden.
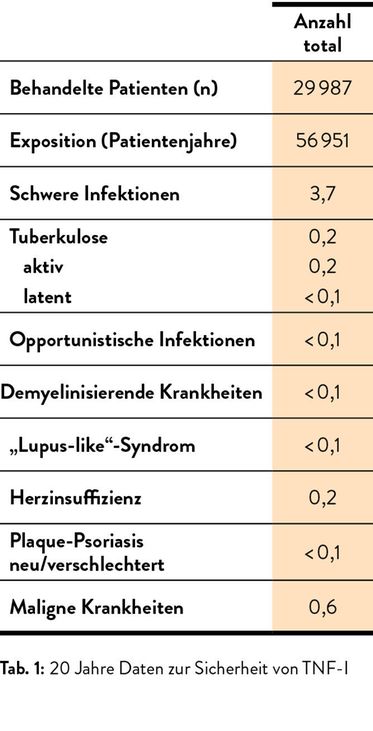
Die Sicherheitsdaten aus knapp 20 Jahren bezüglich der TNF-Inhibitoren sind beeindruckend (Tab. 1). Dies wird auch durch die weltweiten Registerdatenbanken gestützt, in denen Patienten ohne gestraffte Studienprotokolle einfließen. Mittlerweile können auch TNF-alfa-Inhibitoren in der Schwangerschaft verabreicht werden!
… wirklich der Erfolg?
Eine signifikante Besserung tritt aus rheumatologischer Sicht bei ca. 30% der Patienten ein. Das heißt aber auch, dass 70% der Patienten nicht ausreichend von den Therapiemöglichkeiten profitieren. Somit ist der Spielraum für Verbesserungen nach wie vor groß. Es gibt auch keine wirklichen Biomarker, die anzeigen, auf welches Medikament ein Ansprechen zu erwarten ist oder welches sogar Nebenwirkungen aufweisen wird. Somit ist und bleibt der Dialog mit dem Patienten unerlässlich, wie das ja auch in der Lehre gefordert wird.
Die onkologischen Checkpoint-Inhibitoren sind naturgemäß nebenwirkungsbehaftet, aber hier ist anzumerken, dass das Auftreten nicht reflexartig zum Absetzen zwingen muss, da das auch auf ein Ansprechen auf die Therapie hinweist.
… Fragen ist kein Zeichen von Schwäche, sondern von Kompetenz!
Nach zwei Jahren weisen über 40% der Patienten mit entzündlichen Erkrankungen mindestens zwei Komorbiditäten auf. Kardiovaskuläre Ereignisse, Hypertonus, aber auch Diabetes oder Infektionen, bis hin zu Depressionen (Fatigue), um nur eine kleine Auswahl anzuführen, sind Erkrankungen, die Rheumatologen niemals allein kontrollieren werden können.
Die Kontrolle der Grunderkrankung allein ist "zu wenig", denn je mehr Komorbiditäten es gibt, desto geringer ist die Remissionsmöglichkeit.
Lifestyle? Biologika wirken, wieso soll sich der Patient dann ändern?
Schlagzeile: "2 Pikser im Jahr – und das war’s. Neues Wirkprinzip könnte die LDL-Senkung erheblich erleichtern!"
Für Patienten nach Herzinfarkt oder Schlaganfall, bei denen die Kontrolle der Lipide entscheidend für das weitere Überleben ist, ist das eine tolle Option. Nur ab wann darf ein primärer prophylaktischer Einsatz diskutiert werden, wenn diätologische Aufklärungen nicht umgesetzt oder eingehalten werden? Auch für die Gichtarthritis stehen Biologika als deutlich teurere Option zum Kortison zur Verfügung. Wir sprechen dann über Kosten von 12000 Euro für eine (!) Spritze alle 6 bis 8 Wochen. Diese Injektionen sind äußerst wirksam, aber was ist demgegenüber die ärztliche Aufklärung "wert", um Patienten eine Lifestyle-Modifikation näherzubringen?
… müssen es also immer biologische Medikamente sein?
Für die im Alter sehr schmerzhafte Osteoporose sind in den letzten Jahren auch Biologika entwickelt worden, die den Knochenstoffwechsel so beeinflussen, dass das weitere Frakturrisiko massiv gesenkt werden kann. Die oralen Bisphosphonate werden immer mehr diskutiert. Es etablierten sich mittlerweile auch Substanzen, die einen Knochenaufbau induzieren.
Müssen es also immer Biologika sein? Dazu abschließend eine kleine Studie aus Deutschland der Forschungsgruppe von Prof. Uwe Lange aus Bad Nauheim: Er unterteilte seine Klinik in zwei Stockwerke; während im 1. Stock bei Patienten mit Osteoporose die Standardtherapie weitergeführt wurde, wurde im 2. Stock ein spezielles Programm mit Koordination/Balance sowie Kraft und Ausdauer etabliert (Zeitraum: 2 Jahre). Die Knochendichte sowie die Knochenstoffwechselmarker konnten in der intensivierten Therapiegruppe signifikant verbessert werden. Zusätzlich traten deutlich weniger Stürze im 2. Stock auf, was auf die deutlich gesteigerte Stabilität zurückzuführen ist.
Fazit
In der Medizin sollte anerkannt werden, dass eine "frühere" Diagnose nicht immer notwendigerweise "besser" ist, dass "mehr" Behandlung nicht automatisch "effektiver" ist und "erhöhte Sensitivität" von diagnostischen Tests nicht als Synonym für "besseren Erfolg" steht. Es erscheint aber auch nicht gerechtfertigt, biologische Therapien vorzuenthalten.
Wir müssen Krankheit besser vom Krankheitsrisiko unterscheiden. Letztendlich hängt der "eine" Behandlungserfolg nicht nur von zellulären und biologischen Faktoren ab, sondern vielmehr von einem immateriellen Zusammenspiel von Komorbiditäten, psychosozialen Faktoren, Compliance, Überzeugungen und nicht wissenschaftlichen Wahrnehmungen.
Quelle:
Vortrag im Rahmen der AGM, Dezember 2019, Graz

