26. Februar 2024
Fortschritte in der Strahlentherapie
Radiotherapie: das Wichtigste von 2023
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf allgemeineplus.at und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. universimed.com & med-Diplom.at)
2023 wurden einige sehr wichtige Arbeiten publiziert, in denen «rein» strahlentherapeutische Entwicklungen zu einer signifikanten Verbesserung wichtiger Endpunkte geführt haben. Moderne Zielvolumenkonzepte können die Ergebnisse bei Mammakarzinomen und pharyngealen Tumoren verbessern, eine Dosisintensivierung kann die Therapie des kleinzelligen Lungenkarzinoms und die Bemühungen auf dem Gebiet des Organerhalts bei Rektumkarzinomen revolutionieren. Neuere Daten bestätigen den hohen Stellenwert der blasenerhaltenden Radiochemotherapie. Schliesslich setzt moderne Technik mit nur wenigen Sitzungen und minimaler Toxizität neue Standards in der Therapie des Prostatakarzinoms.
Kopf-Hals-Tumoren
Späte, chronische Dysphagie ist eine häufige Toxizität nach kurativer Radio(chemo)therapie von Kopf-Hals-Tumoren. Sie hat einen relevanten negativen Einfluss auf die Lebensqualität der stets wachsenden Population an oft jüngeren Langzeitüberlebenden.
Die britische Gruppe um Chris Nutting vom Royal-Marsden-Krankenhaus, die auch die parotidenschonende intensitätsmodulierte Radiotherapie (IMRT) für die gleiche Indikation etabliert hat, hat im vergangenen Jahr die lang erwarteten Ergebnisse der prospektiven randomisierten Phase-III-Studie zur Konstriktorenschonung publiziert.1 Bei der sogenannten «Dysphagia optimized»(DO)-Methode werden alle Teile der pharyngealen Konstriktormuskulatur ausserhalb des Hochdosisbereichs mithilfe einer IMRT-Planung unter einer bestimmten mittleren Dosisschwelle (50Gy) gehalten. Dies führte nach einer medianen Nachbeobachtungsphase von 39,5 Monaten sowohl subjektiv als auch objektiv zu signifikant niedrigeren Raten an später Dysphagie. Die objektive Evaluation wurde durch verblindete Experten mithilfe des MD-Anderson-Dysphagie-Inventars (MDADI) durchgeführt. Dabei hatten die Patienten der experimentellen DO-IMRT-Gruppe ein Jahr nach Radiotherapie einen signifikant höheren MDADI-Score (p=0,037, primärer Endpunkt) – und das ohne jegliche Einbusse bzgl. sonstiger Toxizität oder Tumorkontrolle.
Damit kann die Dysphagie-optimierte IMRT als neuer Standard in der Bestrahlungsplanung bei pharyngealen Karzinomen deklariert werden.
Mammakarzinom
Die Indikation und der Nutzen einer Bestrahlung der regionalen Lymphabflusswege, also der axillären, supraclaviculären Lymphknoten und der Mammaria-interna-Lymphknoten, waren lange ein ungelöstes Problem der Brustkrebsbehandlung. Grund dafür war die heterogene Datenlage, die teils kontroverse Resultate hinsichtlich des onkologischen Benefits und der Spättoxizität zeigte. Besonders die gefürchtete kardiovaskuläre Spättoxizität nach Bestrahlung der Mammaria-interna-Region führte zu einer schwierigen Abwägung zwischen Risiken und Nutzen. Die raschen Entwicklungen der radiotherapeutischen Techniken und der Systemtherapien über die Jahrzehnte haben die Interpretation der ohnehin heterogenen Daten weiter verkompliziert.
Gegen Ende des Jahres hat die «Early Breast Cancer Trialists’ Collaborative Group» (EBCTCG) die weltweit grösste Metaanalyse von individuellen Patientinnendaten zum Thema publiziert. Eingeschlossen waren Daten von 14324 Frauen und 16 klinischen Studien aus dem Zeitraum von 1961 bis 2018.2 Studien von 1961 bis 1978, die veraltete Bestrahlungstechniken benutzten, wurden separat betrachtet. Diese Studien zeigten teilweise eine erhöhte nichtbrustkrebsspezifische Mortalität.
Anhand der Daten von 12167 Frauen aus der jüngeren Zeit (1989–2008) konnte in dieser Metaanalyse demonstriert werden, dass die Bestrahlung der regionalen Lymphabflusswege (LAW) zu einer signifikanten Reduktion der Gesamtmortalität, der brustkrebsspezifischen Mortalität und der Rezidivrate führte. Genauer betrachtet reduzierte die LAW-Bestrahlung im Gesamtkollektiv das Rezidivrisiko nach 15 Jahren um 2,6%, die Rate an Fernmetastasen um 2,9%, die Mammakarzinomsterblichkeit um 3% und die Gesamtsterblichkeit ebenfalls um 3%.
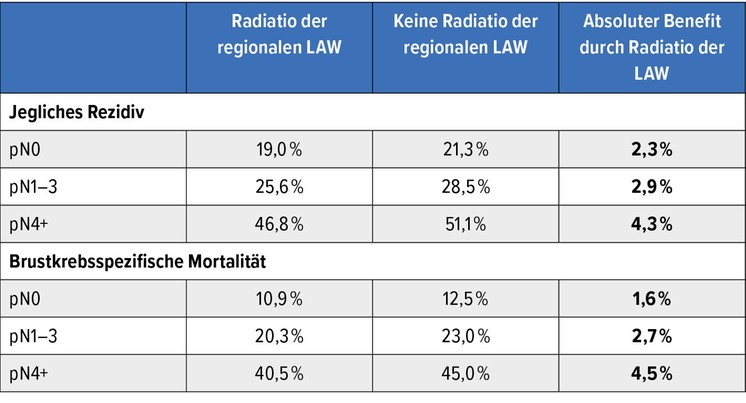
Wichtig dabei ist, dass die Sterblichkeit ohne Rezidiv in beiden Gruppen identisch und durch die zusätzliche Bestrahlung nicht erhöht war. Der absolute Vorteil war dabei nur vom pN-Stadium als einzigem prädiktivem Faktor (Tab. 1) abhängig. Die grosse Mehrheit der Patientinnen bekam sogar eine Axilladissektion und selbst Patientinnen in der pN0-Kategorie scheinen von der regionalen LAW-Bestrahlung zu profitieren.
Eine Volumeneskalation der adjuvanten Radiotherapie unter Inklusion der regionalen LAW soll immer angeboten werden und besonders bei Frauen mit befallenen Lymphknoten indiziert werden. Der absolute Vorteil bezüglich des Gesamtüberlebens mit 3% nach 15 Jahren ist dabei grösser als bei vielen etablierten und zugelassenen Systemtherapien.
Tab. 1: Kumulative 15-Jahres-Risiken mit oder ohne Bestrahlung der regionalen LAW abhängig von der pN-Kategorie. Modifiziert nach EBCTCG2
Kleinzelliges Lungenkarzinom
Die onkologischen Ergebnisse nach initialer Behandlung des kleinzelligen Lungenkarzinoms sind alles andere als zufriedenstellend; und seit Etablierung der simultanen Radiochemotherapie sind zumindest im Stadium «limited disease» kaum Fortschritte zu verzeichnen. Die 5-Jahres-Gesamtüberlebens-Rate beträgt dabei für die Stadien IIB–IIIC etwa 10%. Auch ein potenzieller Vorteil der Immuntherapie verbleibt in Gegensatz zu mehr fortgeschrittenen Stadien unklar und, wenn überhaupt vorhanden, gering.
Vor diesem Hintergrund untersuchte eine chinesische prospektiv-randomisierte Phase-III-Studie die Ergebnisse einer Intensivierung der physikalischen Strahlendosis um 20% in der Erstlinientherapie im Stadium «limited disease». Die Ergebnisse wurden zum ersten Mal beim jährlichen Kongress der amerikanischen Gesellschaft für Radioonkologie (ASTRO) präsentiert.3 Dabei wurden insgesamt 224 Patienten 1:1 zwischen einer Platin-Etoposid-basierten Standardradiochemotherapie, hyperfraktioniert (1,5Gy 2x täglich) bis 45Gy, und der gleichen Behandlung, aber bis 54Gy (1,8Gy, 2x täglich), randomisiert. Dieses intensiver akzelerierte Schema mit Applikation einer höheren physikalischen Dosis in der gleichen Zeitspanne resultiert theoretisch in einer noch höheren biologischen Wirkung. Prophylaktische Ganzhirnbestrahlung wurde für alle ansprechenden Patienten gemäss Empfehlungen appliziert.
Die Ergebnisse waren überzeugend: Das Gesamtüberleben (primärer Endpunkt, median 62,4 vs. 43,1 Monate) und das progressionsfreie Überleben in der experimentellen Gruppe (HR jeweils 0,59 und 0,77) waren signifikant verlängert. Interessanterweise waren dabei die Raten an gefürchteten Toxizitäten, nämlich Ösophagitis und Pneumonitis Grad III–IV, mit jeweils 12–13% und 4,6–6% nicht unerwartet und in beiden Gruppen fast identisch. Diese Daten demonstrieren, dass eine intensive Eskalation der Strahlendosis sowohl durch Erhöhung der physikalischen Dosis als auch Akzelerierung mit verbesserten onkologischen Ergebnissen ohne zusätzliche Nebenwirkungen möglich ist.
Rektumkarzinom
Die Fortschritte in der präoperativen Systemtherapie des Rektumkarzinoms haben in den letzten Jahren zu einer Verbesserung der Remissionsraten und der onkologischen Ergebnisse und sogar zur Frage nach der Notwendigkeit einer Radiotherapie überhaupt im neoadjuvanten Setting geführt. Allerdings konnte auch der Rektumerhalt durch Verzicht auf Operation von einem «akzidentellen» Ereignis zu einem zunehmend erwünschten und erreichbaren onkologischen Ziel avancieren.
In diesem Kontext spielen innovative Radiotherapieschemata eine immer grössere Rolle, wie im Rahmen der prospektiv-randomisierten Phase-III-Studie OPERA gezeigt werden konnte.4 Die französische Gruppe um Jean-Pierre Gerard randomisierte 141 Patienten mit operablem Rektumkarzinom, Stadien cT2–3b cN0-1, 1:1, zwischen einer dosisintensivierten, rein perkutanen Bestrahlung mit 45Gy plus 9Gy Boost simultan zu Capecitabin versus Radiochemotherapie mit 45Gy plus 30Gy, appliziert als Kontakt-Brachytherapie-Boost in drei Sitzungen. Die Teilnehmenden wurden nach T-Kategorie, Tumordurchmesser (<3cm vs. grösser) und Abstand von der Linea anocutanea stratifiziert. Der primäre Endpunkt war der Rektumerhalt nach drei Jahren. Eine totale mesorektale Exzision folgte, wenn kein oder nur partielles Ansprechen nach Radiatio postuliert wurde. Komplette oder fast komplette Remissionen konnten nachbeobachtet werden.
Der Organerhalt war bei 81% aller Patienten im experimentellen Brachytherapie-Arm möglich, versus 59% im perkutanen Arm (p=0,0026, HR: 0,36). Noch höher war die Rate an Rektumerhalt bei den kleinen Tumoren <3cm (97% vs. 63%, p=0,012, HR: 0,07). Die einzige signifikant häufigere, aber nicht höhergradige Toxizität im experimentellen Arm war eine erhöhte Rate an rektalen Blutungen vom Grad I–II (63% vs. 12%).
Diese Raten an Rektumerhalt sind die besten bis jetzt erreichten und die Methode soll bei geeigneten Patienten mit cT2–3-Tumoren und entsprechendem Wunsch angeboten werden.
Blasenkarzinom
Bisherige Versuche für einen prospektiv-randomisierten Vergleich zwischen Zystektomie und blasenerhaltender trimodaler Therapie (transurethrale Resektion gefolgt von Radiochemotherapie) sind an mangelnder Rekrutierung gescheitert. Aus diesem Grund haben Forscher aus den drei weltweit in der Therapie des Blasenkarzinoms führenden Zentren (Boston, Los Angeles, Toronto) ihre Daten zusammengeführt und sowohl nach dem «propensity score matching» (PSM) als auch gemäss «weighted analysis» gewertet.5
Die finale Analyse konnte 722 Patienten identifizieren, die ohne Einschränkungen für beide Modalitäten (Zystektomie oder trimodale Therapie) geeignet wären. Ferner waren ein Stadium T2–4 N0 M0, eine Tumorausdehnung <7cm, solitärer Tumor, maximal unilaterale Hydronephrose, adäquate Blasenfunktion und Fehlen einer extensiven CIS-Komponente Einschlusskriterien. In diesem Kollektiv konnte mit beiden statistischen Methoden kein Unterschied im metastasenfreien Überleben (primärer Endpunkt, 74% vs. 75%) und im krankheitsfreien Überleben (73% vs. 74%) gezeigt werden. Interessanterweise konnte aber mit beiden Methoden ein signifikanter Vorteil hinsichtlich des Gesamtüberlebens zugunsten der trimodalen Therapie beobachtet werden: 77% [72–81] vs. 72% [69–75], HR: 0,75 [0,58–0,97] (p=0,0078, PSM).
Alle Ergebnisse waren konsequent und fast identisch über alle drei beteiligte Zentren. Ferner war eine Salvage-Zystektomie bei nur 13% der Patienten nach trimodaler Therapie überhaupt nötig und diese war in nur 1% der Fälle inkomplett (R1) und mit einer akzeptablen 2,5%igen Mortalität assoziiert. Diese Arbeit liefert die bislang beste Evidenz für die Effektivität einer blasenerhaltenden trimodalen Therapie für selektionierte Patienten. Sie soll allen geeigneten Patienten als Alternative zur Zystektomie angeboten werden.
Prostatakarzinom
Bereits 2022 wurden die Ergebnisse der prospektiv-randomisierten, internationalen Phase-III-Studie PACE-B publiziert. Sie untersuchte die Toxizität bis zu zwei Jahre nach Anwendung einer stereotaktischen Radiotherapie (SBRT) in fünf Fraktionen für Prostatakarzinome der Gruppen mit niedrigem und mittlerem Risiko. Im vergangenen Jahr wurden im Rahmen des jährlichen ASTRO-Kongresses die 5-Jahres-Ergebnisse inklusive biochemischer Kontrolle präsentiert.6
In der Studie wurden insgesamt 874 Patienten mit lokalisiertem Prostatakarzinom, cT1c–cT2c, Gleason ≤3+4, PSA ≤20ng/ml, mit MRI und ohne Androgendeprivation randomisiert. Den Patienten wurde 1:1 eine konventionell fraktionierte bis moderat hypofraktionierte Bestrahlung (d.h. 2–3,1Gy über 4–8 Wochen) oder eine SBRT in nur 5 Sitzungen (36,25Gy und 40Gy auf das klinische Zielvolumen über 1–2 Wochen) zugeteilt. Primärer Endpunkt war der biochemische oder klinische Progress. Die beiden Gruppen waren bezüglich der Patienten und Tumormerkmale gut balanciert. Wichtig ist dabei, zu betonen, dass 91% der Patienten der Gruppe mit intermediärem Risiko angehörten und 82% einen Gleason-Score von 7a hatten. Ausserdem gehörten 42% der Tumoren der Kategorie cT2c an.
Die Studie war positiv, mit einer Ereignisfreiheit bei 95,8% der Patienten im SBRT-Arm und 94,6% im konventionellen Arm. Wichtig dabei ist, dass auch nach fünf Jahren kein signifikanter Toxizitätsunterschied zu verzeichnen war: Grad 2 oder höhere urogenitale Toxizität (G2+ nach RTOG) trat in 3,2% (11/348) im konventionellen Arm und 5,5% (20/363) im SBRT-Arm auf (p=0,14); G2+ gastrointestinale Toxizität bei nur 1/348 im konventionellen Arm und 1/363 im SBRT-Arm (p=0,99).
Diese ersten Langzeitdaten über die extreme stereotaktische Fraktionierung für das lokal begrenzte Prostatakarzinom öffnen den Weg zur Etablierung dieser modernen Technik als neuen Standard mit reduzierter behandlungsassoziierter Belastung für die entsprechenden Patienten.