23. März 2021
Aspergillose pulmonaire invasive (API)
Incidence élevée chez les patients ventilés atteints de Covid-19
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf allgemeineplus.at und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. universimed.com & med-Diplom.at)
Les patients sous assistance respiratoire en soins intensifs pour une maladie à Covid-19 sévère présentent un risque accru d’infections secondaires. En raison du mauvais pronostic, les aspergilloses pulmonaires invasives doivent, chez ces patients, être recherchées tôt et traitées par antimycosiques.
Jusqu’à un tiers des patients hospitalisés pour une maladie à Covid-19 doivent être traités en unité de soins intensifs pour une insuffisance respiratoire secondaire faisant suite à une pneumonite virale.1 Outre un risque accru de co-infection bactérienne, des mycoses secondaires, dont les aspergilloses pulmonaires invasives, sont de plus en plus souvent signalées chez les patients intubés et sous ventilation mécanique.2–5 La survenance d’une telle complication chez les patients atteints de Covid-19 est associée à une mortalité accrue et elle doit donc être diagnostiquée et traitée de façon précoce.
Des études mettent en évidence une incidence élevée chez les patients atteints de Covid-19 sous assistance respiratoire
L’immunocompétence joue un rôle essentiel dans la pathogenèse des maladies associées à l’Aspergillus. Les Aspergillus sont omniprésents dans la nature. Si l’exposition aux spores est généralement inoffensive pour les personnes en bonne santé, elle peut entraîner des aspergilloses invasives engageant le pronostic vital chez les personnes immunodéprimées ou gravement malades.
La survenance d’aspergilloses pulmonaires invasives (API) chez des patients nécessitant des soins intensifs à la suite d’une infection grave par des coronavirus (SARS-CoV, MERS) ou par des virus de la grippe a été signalée.6–8 Dès le début de la pandémie actuelle de coronavirus, des preuves initiales de co-infection par Aspergillus ont été constatées chez des patients atteints de la maladie à Covid-19 sévère dans la région de Wuhan en Chine.9 Entre-temps, des cas rétrospectifs ont été signalés dans plusieurs pays, dont les Pays-Bas, l’Allemagne, la France et la Belgique.2–5 Ils rapportent la survenance d’une API chez 20–35% des patients intubés et ventilés atteints de Covid-19. Une grande étude prospective italienne portant sur 108 patients intubés et ventilés mécaniquement atteints de Covid-19 a fait ressortir une incidence comparable.10
Les conséquences d’une API sont souvent fatales
Comme l’a montré l’étude prospective de Bartoletti et al., la mortalité à 30 jours des patients atteints d’aspergillose pulmonaire associée au Covid-19 (CAPA) était significativement plus élevée que chez les patients ne présentant pas de CAPA (44% contre 19%, p=0,002). La mortalité au cours de cette période était encore plus élevée chez les patients chez qui l’on soupçonnait une aspergillose invasive (74% contre 26%, p<0,001).10 Dans une étude prospective multicentrique récemment publiée portant sur 135 patients du Royaume-Uni traités pour une maladie grave de type Covid-19 avec insuffisance respiratoire en unité de soins intensifs, la mortalité toutes causes confondues était de 38%. Une CAPA avait déjà été diagnostiquée chez 60% des personnes décédées. La mortalité des patients atteints de CAPA variait de 47% à 100%, selon que les patients avaient reçu ou non un traitement antimycosique.11
De nombreux facteurs prédisposent à une aspergillose invasive
Les patients traités en soins intensifs pour une maladie à Covid-19 sévère présentent différents facteurs de risque de mycoses secondaires. Il s’agit notamment d’une ventilation invasive pour cause de syndrome de détresse respiratoire aiguë (SDRA), de l’altération de la réponse immunitaire due à une lymphopénie et d’une réponse inflammatoire systémique exubérante qui entraîne souvent un traitement par immunomodulateurs.12 Une étude récente a identifié la présence d’une affection respiratoire chronique et un traitement par corticostéroïdes comme des facteurs de risque importants d’une API.11 Dans l’essai RECOVERY, le traitement par stéroïdes systémiques a entraîné un bénéfice en termes de mortalité chez les patients atteints de Covid-19 qui étaient sous ventilation mécanique ou avaient reçu une oxygénothérapie, et fait désormais souvent partie du plan de traitement.13
Le rôle de la physiopathologie spécifique du Covid-19 dans le développement d’une API n’est pas clair. Cependant, la lésion directe du tissu pulmonaire par le SARS-CoV-2 et les grandes lésions alvéolaires et interstitielles bilatérales associées favorisent probablement la survenance de mycoses secondaires.12
Un diagnostic difficile
En raison du mauvais pronostic, une API doit être recherchée et traitée précocement chez les patients atteints d’une maladie à Covid-19 sévère.10, 11 C’est particulièrement vrai pour les patients présentant une maladie respiratoire réfractaire sévère ou une détérioration de la fonction respiratoire.11
Cependant, pour différentes raisons, le diagnostic est difficile. Tout d’abord, la détection des signes radiologiques typiques d’une aspergillose invasive, tels que les changements nodulaires ou les cavernes, est souvent difficile ou impossible en raison de l’affection pulmonaire sous-jacente. Ce à quoi il convient d’ajouter que les définitions existantes pour l’investigation des maladies fongiques invasives, telles que celle de l’Organisation européenne pour la recherche et le traitement du cancer/Mycoses Study Group Education and Research Consortium (OERTC/MSGERC) ou celle de l’AspICU (Aspergillus species in intensive care unit patients), présentent plusieurs faiblesses.14, 15 Dans une publication récente, White et al. proposent une stratégie de dépistage complète chez les patients atteints d’une maladie grave de type Covid-19.11 Celle-ci comprend un examen radiologique et une large combinaison de tests sanguins et d’analyses des sécrétions des voies respiratoires inférieures, notamment la PCR d’Aspergillus, le test au galactomannane, le dosage du (1-3)-β-D-glucane, pour la détection indirecte et directe des agents pathogènes (Tab. 1).16
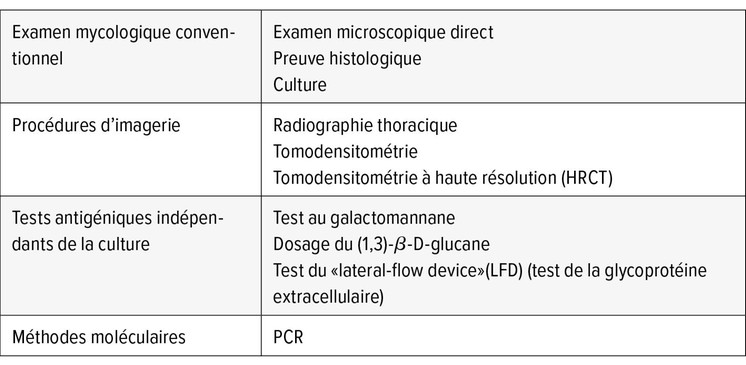
Tab. 1: Méthodes de diagnostic pour la détection d’une aspergillose pulmonaire invasive (API) (d’après Moura et al.)16
Un agent antimycosique éprouvé: l’amphotéricine B liposomale
Plusieurs principes actifs sont disponibles pour le traitement d’une API.17 Un récent consensus d’experts de la European Confederation of Medical Mycology/International Society for Human & Animal Mycology (ECMM/ISHAM) sur la prise en charge de la CAPA recommande que les patients présentant une résistance aux azolés soient initialement traités avec de l’amphotéricine B liposomale (AmBisome®).18
AmBisome® possède un large spectre d’activité antimycosique et est autorisé pour le traitement des mycoses systémiques et/ou profondes sévères causées par des agents pathogènes sensibles à l’amphotéricine B. En outre, le principe actif peut être utilisé pour le traitement empirique des infections fongiques suspectées chez les patients présentant une neutropénie fébrile.19 Après l’administration intraveineuse, l’amphotéricine B se répartit dans les tissus fréquemment affectés par les infections fongiques, où elle exerce un effet fongicide rapide et dose-dépendant.20
L’amphotéricine B a une longue histoire (Fig. 1). Le polyène macrocyclique a été le tout premier principe actif antimycosique et est utilisé pour traiter les infections fongiques invasives depuis le milieu des années 1950. La première formulation de l’amphotéricine B se caractérisait par une bonne efficacité mais était associée à une néphrotoxicité et une hépatotoxicité pertinentes ainsi qu’à des perturbations électrolytiques et à des réactions à la perfusion. Avec l’amphotéricine B liposomale, une nouvelle formulation galénique, dont le profil de sécurité est nettement amélioré par rapport à l’amphotéricine B conventionnelle, est disponible depuis plus de 30 ans.21

Fig. 1: AmBisome®: trois décennies de lutte contre les infections fongiques potentiellement mortelles
Ceci est dû à sa galénique particulière, des liposomes, qui se fixent d’abord à la paroi fongique et sont ensuite transportés à travers la membrane cellulaire, où l’antimycosique déploie finalement son effet.22 Contrairement à l’amphotéricine B classique, l’amphotéricine liposomale reste liée aux liposomes. Dans les études animales, aucune amphotéricine B libre n’a été détectée dans le plasma.19
Pas d’excrétion rénale
L’effet d’un traitement initial par l’amphotéricine B liposomale a été étudié, entre autres, dans l’étude AmBiLoad.23 Cette étude randomisée en double aveugle incluait 201 patients immunodéprimés présentant une maladie invasive due à des moisissures probables ou confirmées, une aspergillose invasive dans 97% des cas. La dose standard approuvée de 3mg/kg/j a permis d’obtenir un taux de réponse de 50% et un taux de survie à 12 semaines de 72% chez ces patients.
L’amphotéricine B liposomale a été utilisée dans des essais cliniques chez des patients présentant une insuffisance rénale préexistante à des doses de 1–5mg/kg/j sans qu’il soit nécessaire d’ajuster la dose ou les intervalles posologiques.19 La néphrotoxicité plus faible est sans doute également due au fait que l’amphotéricine B liposomale, contrairement à la formulation conventionnelle, n’est pas éliminée par les reins. On suppose plutôt que l’amphotéricine B liposomale est éliminée par phagocytose par les macrophages du système réticulo-endothélial. Néanmoins, des effets indésirables, y compris des effets rénaux indésirables, sont possibles pendant le traitement par AmBisome®, en particulier aux posologies élevées.19
Depuis 2010, l’amphotéricine B liposomale figure sur la liste des médicaments essentiels de l’OMS.
Le principal en bref
-
On retrouve une aspergillose pulmonaire invasive pouvant aller jusqu’à un tiers des patients atteints de Covid-19 sous assistance respiratoire.
-
La mortalité liée à une aspergillose associée au Covid-19 peut être réduite par l’instauration précoce d’un traitement antimycosique.
-
Le dépistage recommandé comprend une combinaison de tests sanguins et d’analyses des sécrétions des voies respiratoires inférieures, en plus de l’imagerie.
-
L’amphotéricine B liposomale est un agent antimycosique éprouvé contre les aspergilloses pulmonaires confirmées ou soupçonnées.23
-
En cas d’aspergillose associée au Covid-19 et de résistance aux azolés, l’amphotéricine B liposomale est recommandée comme traitement de première intention.18
Information professionnelle abrégée
AmBisome® COMP: 50mg d’amphotéricine B liposomale/flacon, poudre pour dispersion pour perfusion i.v. IND: Traitement des mycoses systémiques graves et/ou profondes dues à des agents pathogènes sensibles à l’amphotéricine B. Traitement empirique des suspicions de mycose chez les patients neutropéniques fébriles. POS: Mycoses systémiques: 3–5mg/kg/jour. Mucormycoses: 5–10mg/kg/jour, dans certains cas jusqu’à 14mg/kg/jour. Méningites à Cryptococcus chez les patients infectés par le VIH: 6mg/kg/jour. Traitement empirique lors d’une neutropénie fébrile: 3mg/kg/jour. Chez les enfants de 2 ans et plus ainsi que chez les adolescents, la dose à administrer par kg de poids corporel correspond à celle chez les adultes. CI: Hypersensibilité au principe actif ou à l’un des excipients. Mycoses ordinaires superficielles ou mycoses cliniquement indétectables ne pouvant être confirmées que par des tests sanguins ou cutanés. MEG: En cas de réaction anaphylactique sévère, arrêter la perfusion immédiatement. On a constaté de la fièvre et des frissons. En particulier, contrôler régulièrement la fonction rénale et l’équilibre électrolytique. En cas d’altération de la fonction rénale diminuer la posologie ou interrompre le traitement. Mucormycoses: des doses supérieures de 5mg/kg/jour ne doivent être utilisées qu’après une évaluation attentive du rapport bénéfice-risque dans chaque cas. Des cas de toxicité pulmonaire aiguë ont été rapportés chez des patients auxquels de l’amphotéricine B avait été administrée pendant une perfusion de leucocytes. IA: L’administration concomitante de principes actifs antinéoplasiques peut accroître les risques de néphrotoxicité, de bronchospasme et d’hypotension. Peut potentialiser l’effet toxique de la flucytosin. Peut potentialiser l’effet des glucosides digitaliques ou des myorelaxants. L’administration concomitante de corticostéroïdes ou de corticotrophine (ACTH) peut potentialiser l’hypokaliémie. L’administration concomitante d’AmBisome et d’autres médicaments néphrotoxiques peut augmenter le risque de toxicité rénale. G/A: Administration uniquement en cas de nécessité absolue. EI: Les plus fréquents: hypokaliémie, nausées, vomissements, pyrexie, frissons. Catégorie de remise: A. TAMM: Gilead Sciences Switzerland Sàrl, Adresse postale: General-Guisan-Strasse 8, 6300 Zug. Veuillez consulter www.swissmedicinfo. ch pour l’information professionnelle non abrégée.
Mise à jour de l’information: Mars 2020.
Article sponsorisé
Avec l’aimable soutien de Gilead Sciences Switzerland Sàrl