24. Dezember 2020
Osteoporose bei Diabetes mellitus
Diagnose und Management
Patienten mit Diabetes haben ein erhöhtes Risiko für Fragilitätsfrakturen, wobei die Pathophysiologie dahinter unklar und vermutlich multifaktoriell ist. Bei der Wahl der antihyperglykämischen Therapie sollen daher Substanzen mit nachgewiesenem negativem Effekt auf den Knochen nicht zum Einsatz kommen. Bei Vorliegen einer Fragilitätsfraktur ist auf jeden Fall – unabhängig von allen vorliegenden Befunden – eine langfristige spezifische osteologische Therapie indiziert.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf allgemeineplus.at und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. universimed.com & med-Diplom.at)
Diabetes mellitus und Osteoporose zählen zu den häufigsten chronischen Erkrankungen und kommen deshalb beide häufig bei ein und demselben Individuum vor, weshalb davon ausgegangen wird, dass sie in Zusammenhang stehen. Da die Prävalenz beider mit steigendem Alter zunimmt, wird in Anbetracht der Altersstruktur unserer Bevölkerung ihre Häufigkeit zunehmen. Die glykämische Kontrolle ist wichtig für die Beurteilung des individuellen Frakturrisikos. Eine schlechte glykämische Kontrolle hat einen negativen Einfluss auf die Mikroarchitektur des Knochens mit mikrovaskulären Komplikationen in diesem Organsystem.
Einfluss der Behandlung des Diabetes auf das Frakturrisiko
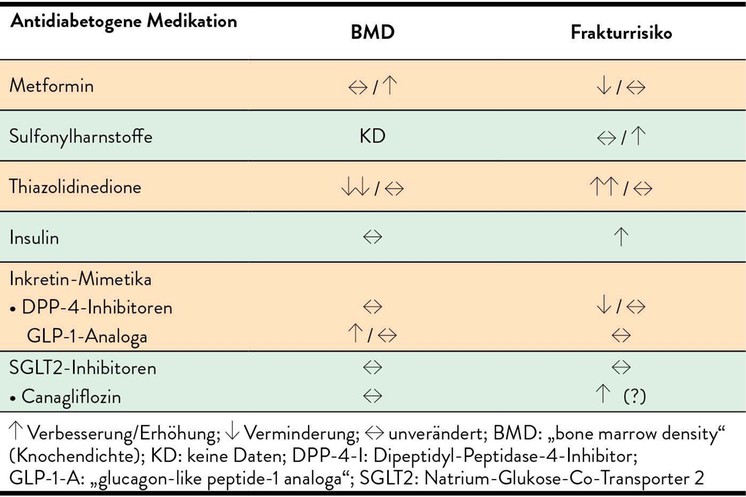
Das Verhältnis zwischen Diabetes und Knochenfragilität und die Identifizierung jener Patienten mit einem erhöhten Risiko für Frakturen werden zusätzlich durch den Einfluss antidiabetogener Medikamente auf das Skelett beeinflusst (Tab. 1).
Tab. 1:Einfluss antidiabetogener Medikamente auf die Knochendichte („bone mineral density“; BMD) und das Frakturrisiko bei Patienten mit Typ-2-Diabetes
Diagnostik
DXA-Knochendichtemessung
Die Knochendichtemessung mittels DXA („dual energy X-ray absorptiometry“) ist nach wie vor der Goldstandard in der Osteoporosediagnostik. Wie von der WHO 1994 festgelegt definiert ein T-Score von ≤–2,5 die Erkrankung, jedoch nicht die individuelle Interventionsschwelle. Die Mehrzahl der Studien bei Patienten mit Diabetesmellitus Typ 1(T1DM) zeigt, dass die Knochendichte („bone mineral density“; BMD) bei dieser Patientenpopulation deutlich vermindert ist. Patienten mit einem Diabetes mellitus Typ 2(T2DM) haben in der Regel eine 5–10% höhere BMD im Vergleich zur nichtdiabetischen, gesunden Population.
Mit dem Trabecular Bone Score (TBS) steht eine Methode zur Verfügung, um aus einer zweidimensionalen DXA-Untersuchung Informationen über die Knochenmikrostruktur der Lendenwirbelsäule zu generieren.
Mikroarchitektur und Knochenqualität
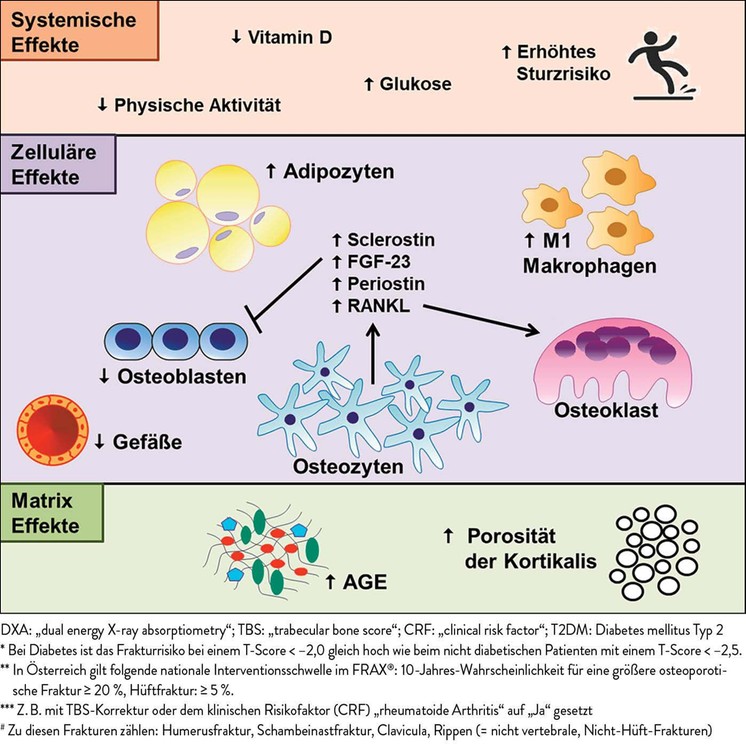
Es findet sich bei T2DM eine verschlechterte Mikroarchitektur. Die Trabekel beim T2DM sind im Vergleich zum nichtdiabetischen Patienten eher hypertrophiert. Im trabekulären Netzwerk finden sich allerdings auch größere Löcher, zusätzlich ist die kortikale Porosität gegenüber Patienten ohne T2DM um bis zu 16% erhöht. Die strukturelle Alteration mit hoher Heterogenität ist an der endokortikalen Übergangszone besonders ausgeprägt („Trabekularisierung der Kortikalis“). Zusätzlich besteht eine strukturelle Einschränkung als Ausdruck veränderter Kollagenverlinkungen in der Knochenmatrix aufgrund vermehrter AGE („advanced glycation endproducts“) (Abb. 1).
Basisprophylaxe mit Vitamin D und Kalzium
Eine ausreichende Versorgung mit Vitamin D ist eine wichtige Voraussetzung für die Knochengesundheit. Eine 25-OH-Vitamin-D-Serumkonzentration <20ng/ml (50nmol/l) ist mit einem erhöhten Risiko für proximale Femurfrakturen und nichtvertebrale Frakturen verbunden.
Zur Therapie eingesetzt wird Cholecalciferol (Vitamin D3); 1μg Vitamin D3 entspricht dabei 40IE Vitamin D3. Die Einnahme soll mit den Mahlzeiten erfolgen, da dies die Resorption verbessert. Die Tagesdosis (z.B. 800IE) kann auch als Wochenäquivalent gegeben werden (5600IE einmal wöchentlich).
Eine ausreichende Kalziumzufuhr ist primär über die Nahrung sicherzustellen.
Spezifische Osteoporosetherapie bei Diabetes
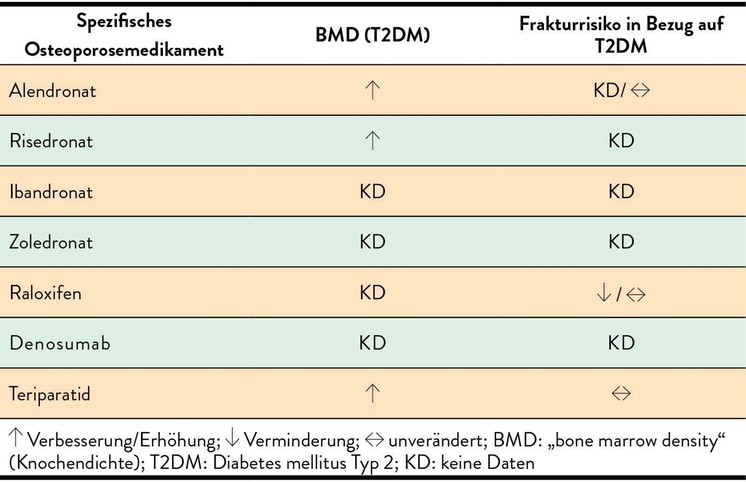
Grundsätzlich sind sämtliche Medikamente zur Behandlung der Osteoporose auch bei Patienten mit einem manifesten Diabetes möglich und zugelassen. Die Effekte einiger dieser Medikamente auf die BMD und das Frakturrisiko sind in Tabelle 2 dargestellt.
Tab. 2: Effekte spezifischer Osteoporosemedikamente bei Patienten mit Typ-2-Diabetes auf die Knochendichte und das Frakturrisiko
Bisphosphonate
Bisphosphonate (Alendronat, Risedronat, Ibandronat, Zoledronat) sind potente Inhibitoren der Knochenresorption. Sie werden an metabolisch aktiven Umbaueinheiten im Knochen abgelagert und bewirken eine Apoptose von Osteoklasten. Die Resorptionsaktivität wird im Gesamtskelett deutlich gedämpft und das Frakturrisiko reduziert.
Oral werden Bisphosphonate nur in geringem Ausmaß (maximal 3%) resorbiert. Bei intravenöser Bisphosphonatgabe kann, überwiegend bei erstmaliger Verabreichung, eine sogenannte Akutphasereaktion auftreten. Bei allen Bisphosphonaten stellen die Hypokalzämie, eine erhebliche Nierenfunktionseinschränkung oder eine Gravidität eine Kontraindikation dar. Das Auftreten von atypischen Femurfrakturen ist sehr selten. Kiefernekrosen sind bei dieser für Osteoporose zugelassenen Therapie eine ebenfalls sehr seltene Nebenwirkung.
Denosumab
Denosumab ist ein monoklonaler Antikörper gegen RANKL, der die Reifung und Aktivierung der Osteoklasten hemmt. Er wird alle sechs Monate subkutan verabreicht und nicht renal eliminiert. Studiendaten und Biopsien von über zehn Jahren Behandlungsdauer zeigen eine anhaltende Reduktion des Frakturrisikos.
Raloxifen
Raloxifen ist ein selektiver Östrogenrezeptor-Modulator (SERM), der die Knochenresorption hemmt und das Frakturrisiko für vertebrale Frakturen reduziert (nicht für nichtvertebrale Frakturen und proximale Femurfrakturen). Ein bedeutender zusätzlicher Effekt ist die Reduktion des relativen Risikos für ein invasives (Östrogenrezeptor-positives) Mammakarzinom um 79%. Eine unerwünschte Nebenwirkung ist die Erhöhung des thromboembolischen Risikos.
Teriparatid
Teriparatid, ein aminoterminales Fragment des Parathormons, wird einmal täglich subkutan über 24 Monate angewandt. Der osteoanabole Effekt beruht auf einer Beschleunigung der Reifung und Stimulierung von Osteoblasten. Im Anschluss an die anabole Reaktion des Knochens kommt es nach Beendigung der Teriparatidtherapie wiederum zu einem gesteigerten Knochenabbau, weshalb eine sofortige Anschlussbehandlung mit einem Antiresorptivum (Bisphosphonat, Denosumab, SERM) unbedingt notwendig ist.
Romosozumab
Romosozumab ist ein humanisierter IgG2-Antikörper gegen Sclerostin. Die natürliche Hemmung des Osteoblasten wird blockiert, dies führt zu einem sehr raschen Anstieg der BMD. Die Dosis beträgt 210mg s.c. 1x/Monat für insgesamt zwölf Monate. Der Antikörper ist zugelassen für die postmenopausale Osteoporose mit hohem Frakturrisiko. Derzeit laufen die Preisverhandlungen. Im Anschluss ist wie bei Teriparatid eine sofortige Anschlussbehandlung mit einem Antiresorptivum notwendig.
Management einer erhöhten Knochenfragilität bei Diabetes
BMD-Interventionsschwelle
Aktuell wird bei Diabetespatienten eine Anhebung der Interventionsschwelle auf einen T-Score von –2,0 an der Lendenwirbelsäule (kumulativ L1–L4) oder an der Hüfte (Schenkelhals bzw. gesamte Hüfte) empfohlen.
FRAX®
Das „fracture risk assessment tool“, kurz FRAX®, ist ein computerbasierter Algorithmus zur Berechnung zweier Risikowerte: zum einen der 10-Jahres-Wahrscheinlichkeit für alle osteoporotischen Frakturen und zum anderen der 10-Jahres-Wahrscheinlichkeit für eine osteoporotische Hüftfraktur. Entsprechend der Österreichischen Leitlinie zur Behandlung der Osteoporose wird ab einem Risiko von (a) ≥20% bzw. (b) ≥5% prophylaktisch eine knochenspezifische Therapie empfohlen.
Diabetes per se ist im FRAX® kein eigener klinischer Risikofaktor (CRF). FRAX® bietet aber die Möglichkeit, die BMD-Werte mittels TBS-Korrektur zu rechnen. Vor allem bei T2DM führt dies zu einer Verbesserung der Vorhersagewahrscheinlichkeit.
Möglichkeiten, im FRAX® die Vorhersagewahrscheinlichkeit zu optimieren, sind:
-
die Erhöhung des Patientenalters um 10 Jahre, da der Risikofaktor Diabetes bei dieser Korrektur in etwa dem Risikofaktor Alter (als etablierter CRF im FRAX®) entspricht;
-
die Verminderung des gemessenen T-Scores am Schenkelhals um 0,5 Standardabweichungen zu verringern (z.B. T-Score –2,4 statt den tatsächlich gemessenen –1,9);
-
die rheumatoide Arthritis als CRF anzugeben.
Der Untersucher sollte sich für eine der drei Möglichkeiten entscheiden, jedoch nicht alle drei Optionen verwenden.
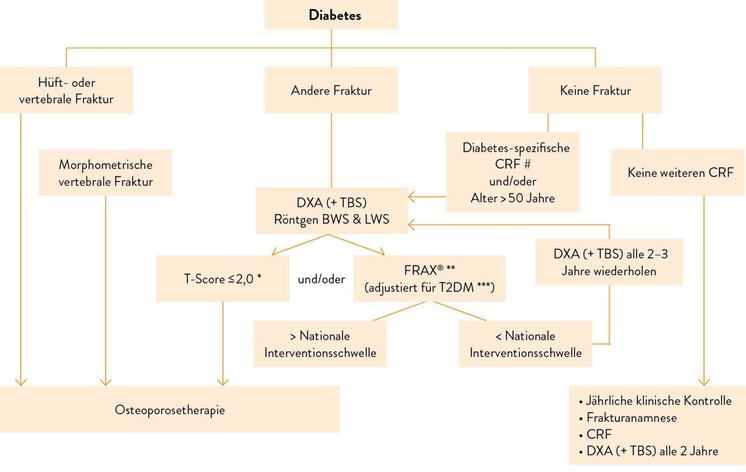
Eine Übersicht zur Evaluation des Frakturrisikos bei Diabetespatienten ist in Abbildung 2 dargestellt.
Literatur: beim Verfasser