NOAKs als Sekundärprophylaxe bei Schlaganfall
Der nachfolgende Artikel macht Allgemeinärzte mit dem sicheren Umgang mit nicht-Vitamin-K-abhängigen oralen Antikoagulanzien (NOAKs) vertraut. Neben allgemeinen Informationen zu Dosierung und Indikation der NOAKs wird das Management in speziellen Situationen wie Blutungskomplikationen, Verhalten bei Operationen oder im akuten Schlaganfall besprochen. Ferner wird auch auf Vorhofflimmern im Allgemeinen sowie auf Alternativen zu einer Antikoagulation eingegangen.
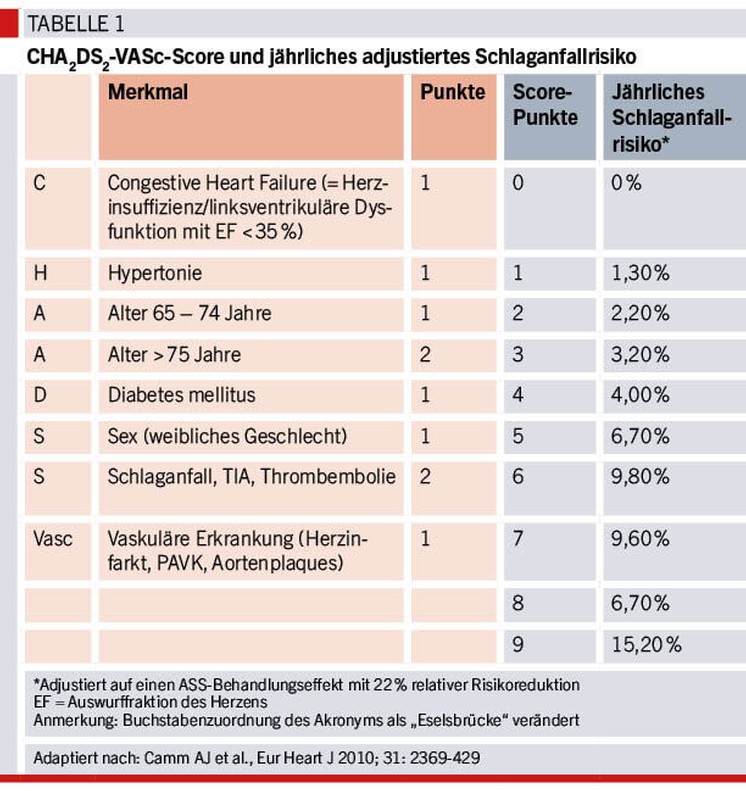
Vorhofflimmern (VHF) ist eine häufige Herzrhythmusstörung, die mit erhöhter Mortalität, reduzierter Lebensqualität und genereller Leistungsschwäche durch eine verminderte Auswurfleistung des Herzens einhergeht. Die Prävalenz bei über 20-Jährigen beträgt etwa 3%, jeder Vierte entwickelt im Laufe seines Lebens ein Vorhofflimmern. Neben dem zunehmenden Alter können auch vaskuläre Risikofaktoren, Herzinsuffizienz, koronare Herzerkrankung, Klappenschäden und Niereninsuffizienz das Risiko, ein Vorhofflimmern zu entwickeln, steigern. Etwa 20 bis 30% aller Schlaganfälle werden durch diese Art der Rhythmusstörung verursacht. Das jährliche Risiko, einen Schlaganfall unter Vorhofflimmern zu erleiden, kann gut mit dem CHA2DS2VASc-Score abgeschätzt werden (Tab. 1). Bei einem CHA2DS2VASc-Score von ≥2 bei Männern und ≥3 bei Frauen besteht die Indikation für eine Antikoagulationsbehandlung. Diese soll auch für jene mit einem CHA2DS2-VASc-Score von 1 bei Männern und 2 bei Frauen in Betracht gezogen werden.1, 2
Die ersten Cumarine (Vitamin-K-antagonistische orale Antikoagulanzien: Warfarin, Phencoumaron, Acenocoumarol) wurden in den 1950er-Jahren als Rattengift und deutlich später auch zur Blutverdünnung beim Menschen eingesetzt. Seit 1989 belegt eine Vielzahl von Studien einen deutlichen Effekt der Cumarine zur Primär- und Sekundärprävention des Schlaganfalls bei Vorhofflimmern mit einer relativen Risikoreduktion von etwa 60% gegenüber Placebo.3 In derselben Metaanalyse wurde eine relative Risikoreduktion von rund 20% durch Thrombozytenfunktionshemmer von grenzwertiger Signifikanz gegenüber Placebo errechnet. Die Entwicklung der direkten spezifischen oralen Thrombin- und Faktor-Xa-Inhibitoren zur oralen Antikoagulation stellt sicherlich eine der wichtigsten pharmakologischen Errungenschaften in der Primär- und Sekundärprävention von Schlaganfällen der letzten 20 Jahre dar. In Anbetracht der Tatsache, dass diese Substanzen seit 2004 beim Menschen eingesetzt werden, wurde die Bezeichnung „neue orale Antikoagulanzien“ durch „Nicht-Vitamin-K-abhängige Orale AntiKoagulanzien“ (NOAK) ersetzt. Zwischenzeitlich wurde auch vorübergehend der Terminus „Direkte Orale AntiKoagulanzien“ (DOAK) verwendet und taucht immer wieder in der Literatur auf.
Zugelassene NOAKs
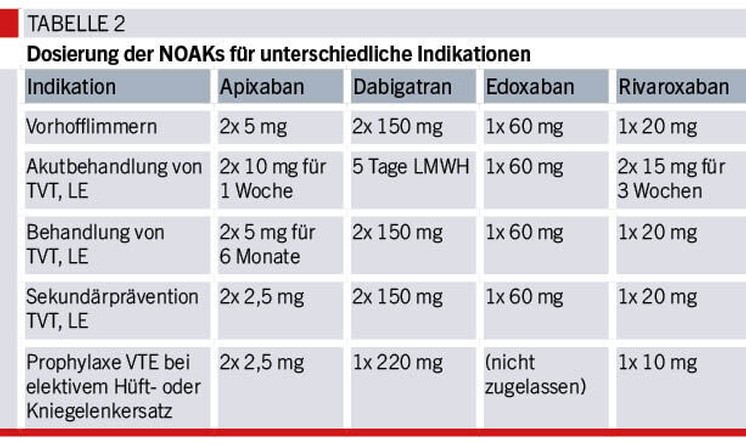
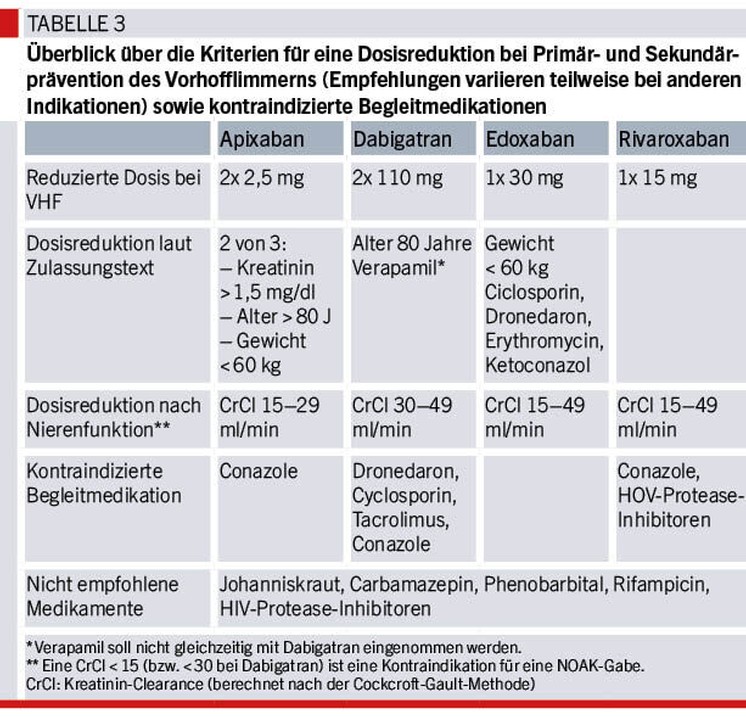
Derzeit sind vier unterschiedliche NOAKs für die Primär- und Sekundärprophylaxe von Schlaganfällen bei Vorhofflimmern zugelassen: Dabigatran ist ein direkter Thrombin-(Gerinnungsfaktor-IIa-)Inhibitor. Apixaban, Edoxaban und Rivaroxaban hemmen den aktivierten Gerinnungsfaktor X (Faktor Xa). Die Zulassung beschränkt sich auf „nicht valvuläres“ Vorhofflimmern, sodass bei Vorhofflimmern und bei mechanischem Klappenersatz, mittel- bis höhergradigen Mitralstenosen sowie die ersten Monate nach einer Klappenoperation mit oder ohne biologische Klappenprothese weiterhin Vitamin-K-Antagonisten zur Anwendung kommen. Wenige Stunden nach der ersten Einnahme eines NOAK ist der volle antikoagulatorische Effekt erreicht. Eine überlappende Behandlung mit niedermolekularem Heparin ist im Gegensatz zu einem Behandlungsbeginn mit Cumarinen deshalb nicht notwendig. Im Unterschied zu den Vitamin-K-Antagonisten wird die individuelle Dosis nicht nach Blutwerten, sondern nach Indikation, Alter, Nierenfunktion, Gewicht und Begleitmedikation angepasst. Tabelle 2 gibt einen Überblick über die zugelassenen Dosierungen bei den unterschiedlichen Indikationen. Für die Neurologie sei hier besonders auf die unterschiedliche Dosierung bei Vorhofflimmern und bei der Sekundärprävention der tiefen Venenthrombose von Apixaban nach sechs Monaten verwiesen, da diese gelegentlich bei paradoxer Embolie und persistierendem Foramen ovale zur Anwendung kommen könnte. In einer kleinen Studie (RE-SPECT CVT) wurde Dabigatran mit Cumarinen bei 120 Patienten mit zerebraler Hirn- und Sinusvenenthrombose verglichen.4 Unter beiden Behandlungen traten sehr wenig schwere Blutungen (eine im Dabigatran-, zwei im Cumarin-Arm) und keine venöse Thromboembolie auf. Eine Zulassung für die Behandlung der zerebralen Hirn- und Sinusvenenthrombose besteht derzeit nicht. Dabigatran wird vereinzelt in Zentren mit hoher Expertise in der Sekundärprophylaxe von unkomplizierten Hirn- und Sinusvenenthrombosen eingesetzt. Tabelle 3 gibt einen Überblick über die wichtigsten Gründe für eine Dosisreduktion bei den unterschiedlichen NOAKs. Eine umfassende Übersicht über Arzneimittelinteraktionen der NOAKs findet sich in der Literatur.5
Auswahl eines NOAK
Grundsätzlich sind alle vier zugelassenen NOAKs hervorragende Medikamente. Allen gemeinsam ist, dass sie in der Primär- und Sekundärprävention des Schlaganfalls bei VHF nicht schlechter sind als die Cumarine. Dabigatran ist in der Dosierung 2x 150mg sogar besser (wobei die Studienpopulationen der randomisierten Studien unterschiedlich waren und die Patienten in der Zulassungsstudie von Dabigatran insgesamt leichtere Schlaganfälle hatten). Die intrazerebralen Blutungskomplikationen sind unter allen NOAKs gegenüber den Cumarinen reduziert bzw. bei Dabigatran in der Dosierung 2x 150mg gleich hoch. Die Häufigkeit von extrazerebralen Blutungen ist bei NOAKs und Cumarinen gleich hoch. Die Wirksamkeit aller Substanzen wurde in qualitativ hochwertigen, großen, randomisierten, kontrollierten Zulassungsstudien nachgewiesen. Hierbei wurde das jeweilige NOAK mit dem Cumarin Warfarin verglichen. Es existieren keine randomisierten Studien, die die Effektivität der einzelnen NOAKs untereinander vergleichen, und auch die individuellen Patientendaten der Zulassungsstudien wurden nie zusammen analysiert, sodass es unmöglich ist, Empfehlungen abzugeben, welches der NOAKs das beste ist. Eine Vielzahl von Metaanalysen der publizierten Zulassungsstudien hat versucht, indirekte Vergleiche anzustellen.5–7 Ferner wurden von allen Substanzen sogenannte Real-World-Daten veröffentlicht.8–10 Dabei handelt es sich meist um Daten aus großen Versicherungsdatenbanken, aus denen die Effizienz und Komplikationsraten der unterschiedlichen oralen Antikoagulationen berechnet wurden. Diese sind zwar wichtig, um das Sicherheitsprofil der NOAKs im „echten Leben“ zu beweisen, können jedoch nur inkomplett die vermutlich geringen Unterschiede zwischen den einzelnen Substanzen darstellen, da die ärztliche Entscheidung für die eine oder andere Substanz in diesen Registern nicht zufällig erfolgt. Dementsprechend sind die Anmerkungen zu den einzelnen Substanzen nicht immer auf einer hohen Evidenzstufe angesiedelt.
Apixaban wird zweimal täglich eingenommen. Die Metaanalysen und Real-World-Daten weisen auf ein hohes Sicherheitsprofil bei hoher Wirksamkeit hin.8, 9
Dabigatran wird zweimal täglich eingenommen und weist eine hohe Wirksamkeit bei gutem Sicherheitsprofil auf. In der hohen Dosis (2x 150mg) ist die Substanz effizienter in der Verhinderung von Schlaganfällen als Warfarin bei gleicher Blutungskomplikationsrate, in der niedrigeren Dosis (2x 110mg) gleich effizient bei geringerer Blutungskomplikationsrate. Mit Idarucizumab steht ein hocheffizientes, sicheres Antidot zur Verfügung. Dabigatran wird in relativ große Kapseln verpackt und beinhaltet Weinsäure, die zu Dyspepsien führen kann. Eine vermehrte Rate an gastrointestinalen Blutungen konnte in den Real-World-Daten und Metaanalysen nicht nachgewiesen werden.8, 9
Edoxaban wird einmal täglich eingenommen. Die Metaanalysen der Zulassungsstudien weisen auf eine gute Wirksamkeit und ein hohes Sicherheitsprofil im Vergleich mit Warfarin hin. In einer explorativen Datenanalyse der Zulassungsstudie wurde der Verdacht auf eine verringerte Wirksamkeit bei einer Kreatinin-Clearance von >95ml/min gestellt.11 Deshalb wird im Zulassungstext der FDA in den USA die Gabe von Edoxaban bei Patienten mit Vorhofflimmern und einer Kreatinin-Clearance von >95ml/min nicht empfohlen. Diese Bedenken werden von der europäischen Zulassungsbehörde nicht geteilt. Real-World-Daten unterstreichen auch hier die Sicherheit des Präparates.10 Ein spezifisches Antidot ist noch nicht zugelassen.
Rivaroxaban wird einmal täglich eingenommen und weist eine gute Wirksamkeit auf. Da die Substanz bereits in anderen Indikationen seit langer Zeit in Verwendung ist, besteht in der Ärzteschaft die meiste Erfahrung im Umgang damit. Metaanalysen und Real-World-Daten liefern Hinweise auf ein ähnliches Risiko von schweren Blutungen wie bei Warfarin.8, 9
Betrixaban, ein oraler Faktor-Xa-Inhibitor, ist nur in den USA für die Thromboseprophylaxe bei hospitalisierten Patienten mit erhöhter Thromboseneigung zugelassen. Eine Phase-II-Studie zum Vergleich mit Warfarin bei Vorhofflimmern ist abgeschlossen.
Betreuung von Patienten unter NOAK-Behandlung
Aufgrund des deutlich einfacheren Managements von NOAKs verglichen mit den Cumarinen besteht die Gefahr, Patienten nicht so ausführlich aufzuklären. Die Substanzen sind hocheffizient, aber auch nicht ungefährlich (gleiche systemische Blutungsrate wie Cumarine). Jede Patientin/jeder Patient muss über die Blutungsneigung aufgeklärt werden und einen Medikamentenpass erhalten. Im Verlauf sollten die Nieren- und Leberwerte sowie ein Blutbild mindestens einmal pro Jahr (bei älteren Patienten alle sechs Monate) bestimmt werden. Wenn die Nierenfunktion ≤60 ml/min ist, sollten die Kontrollen engmaschiger (CrCl geteilt durch zehn in Monaten, z. B. bei einer CrCl von 40 alle vier Monate) erfolgen.5 Ein Monitoring des Therapieeffekts mit spezifischen Tests ist nicht notwendig. Die Stürze unter Cumarin-Behandlung gehen mit einem erhöhten Risiko von intrazerebralen Hämatomen einher. Dennoch profitieren diese Patienten aufgrund des reduzierten Schlaganfallrisikos von der Antikoagulation.12 In der Zulassungsstudie von Edoxaban war der Therapieeffekt in der Subgruppe von Patienten mit Stürzen nicht unterschiedlich zu jenen ohne Stürze.13 Insgesamt stellen Stürze per se keine Kontraindikation für eine Antikoagulation dar.
Abb. 1 a und b: MRT-Aufnahmen von kardioembolischen Ischämien: Die kleinen hellen Flecken zeigen frische Ischämien in verschiedenen Gefäßterritorien.
Alternativen zu einer NOAK-Therapie
Derzeit besteht weitgehender Konsens, dass Patienten mit Vorhofflimmern unter Behandlung mit Vitamin-K-Antagonisten nicht auf eine NOAK-Behandlung umgestellt werden müssen, wenn eine ausreichende Zeit im INR-Zielbereich gegeben ist. Acetylsalicylsäure (ASS) zur Primär- und Sekundärprävention eines Schlaganfalls bei Vorhofflimmern wird von der Europäischen Kardiologischen Gesellschaft nicht mehr empfohlen.1 Dies basiert auf Metaanalysen der Studien mit Warfarin, ASS und Placebo, die einen lediglich moderaten ASS-Effekt gezeigt haben. Blutungskomplikationen unter ASS nehmen mit zunehmendem Alter auch beträchtlich zu.14 In einer randomisierten Studie, in der Patienten, bei denen eine Kontraindikation für eine orale Antikoagulation mit Cumarinen bestand, zu Apixaban oder ASS randomisiert wurden, waren die Blutungskomplikationen in beiden Therapiearmen nicht unterschiedlich, bei deutlich besserer Wirksamkeit von Apixaban.15
Der Verschluss des linken Herzohrs mittels eines endovaskulär eingebrachten Medizinprodukts ist in Europa zugelassen. Eine gemeinsame Analyse zweier kleiner randomisierter Studien und Registerdaten weist auf eine ähnliche Wirksamkeit wie Vitamin-K-Antagonisten hin.16 Leider wurden die Studien nicht an der potenziellen Zielgruppe, also Patienten mit einer Kontraindikation für eine orale Antikoagulation, durchgeführt. Auch bei dieser Prozedur muss eine gewisse Zeit lang antikoaguliert werden und eine langfristige Thrombozytenfunktionshemmung möglich sein. Der chirurgische Verschluss bzw. die Ausschaltung des linken Herzohrs ist ebenfalls möglich. Von der Europäischen Kardiologischen Gesellschaft wird auch nach Verschluss bzw. Ausschaltung des linken Herzohrs eine orale Antikoagulation bei Vorhofflimmern empfohlen. Dieser Eingriff bzw. der interventionelle Herzohrverschluss kann bei Patienten mit Vorhofflimmern und absoluter Kontraindikation für eine langzeitige orale Antikoagulation in Einzelfällen erwogen werden.1 Derzeit laufen mehrere Studien, die eine NOAK-Behandlung mit einem interventionellen Herzohrverschluss vergleichen. Die PRAGUE-17-Studie wurde vor kurzem publiziert.17 Hier war bei Patienten und Patientinnen mit einem hohen Schlaganfall- und Blutungsrisiko der interventionelle Herzohrverschluss gleich effizient wie eine NOAK-Therapie. Da bei der Intervention etwa 5% Komplikationen auftraten, sollte die Interventionstechnik noch verbessert werden.
Wann kann nach einem ischämischen Schlaganfall mit einem NOAK begonnen werden?
Bei etwa 10% aller Schlaganfälle wird ein vorher nicht bekanntes Vorhofflimmern festgestellt. Hier stellt sich natürlich die Frage, wie früh man nach dem Ereignis mit einer oralen Antikoagulation beginnen kann. In einem Cochrane-Review über sehr frühe Antikoagulation nach einem Schlaganfall mit Vitamin-K-Antagonisten und Heparinen konnte grundsätzlich gezeigt werden, dass zwar das Risiko eines erneuten Schlaganfalls (oder einer Lungenembolie) reduziert ist, aber das Blutungsrisiko erhöht wird.18 Da alle Studien mit NOAKs Patienten frühestens zwei Wochen nach einem Schlaganfall oder einer transitorischen ischämischen Attacke (TIA) eingeschlossen haben, gibt es nur Expertenmeinungen zu diesem Thema (Abb. 2).1 Bei einer TIA wird empfohlen, am Folgetag mit der Antikoagulation zu beginnen. Bei einem ischämischen Schlaganfall sollte in Abhängigkeit von der Infarktgröße drei bis zwölf Tage zugewartet werden, wobei bei mittlerer oder großer Schlaganfallausdehnung vorher eine hämorrhagische Transformation mittels zerebraler Bildgebung ausgeschlossen werden muss. Für Neurologen ist es sicherlich sinnvoller, die Ausdehnung des Schlaganfalls im CT oder MRT statt des klinischen Erscheinungsbildes, gemessen anhand des NIHSS, für die Entscheidung heranzuziehen. Da in der Akutphase eines Schlaganfalls das Rezidivrisiko unter 0,1% pro Tag liegt, erscheint es auch gerechtfertigt, bei Unsicherheit einige Tage zusätzlich zu warten, ehe eine orale Antikoagulation begonnen wird.19
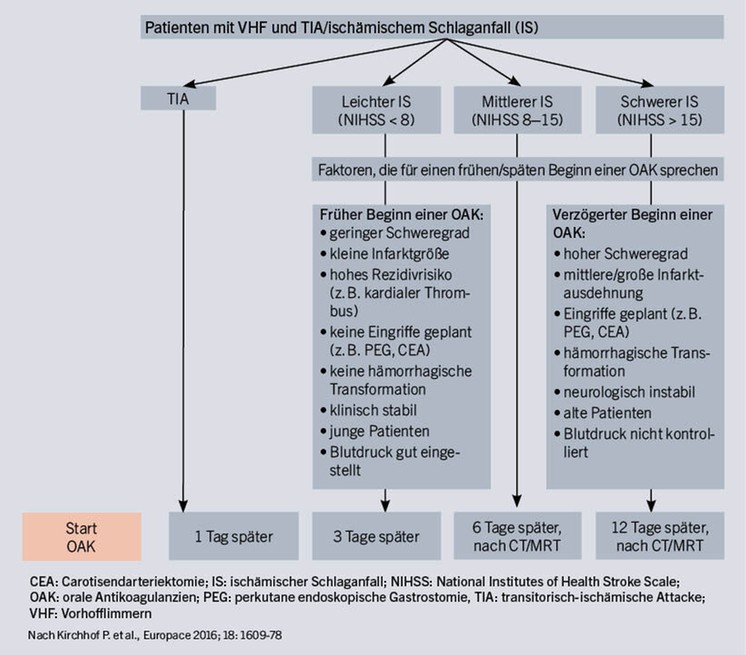
Abb. 2: Therapiealgorithmus für den Beginn mit einer oralen Antikoagulation nach Schlaganfall
Wann kann nach einem intrazerebralen Hämatom mit einem NOAK begonnen werden?
Eine häufig gestellte Frage ist, ob man nach einem blutigen Schlaganfall (intrazerebrales Hämatom, ICH) überhaupt eine Antikoagulation beginnen kann, und vor allem, wann dies sicher möglich ist. Natürlich gibt es zu dieser Fragestellung auch keine randomisierten Studien, sodass diese Entscheidung interdisziplinär unter Einbindung von Neurologen, Radiologen, Kardiologen und Neurochirurgen getroffen und mit dem Patienten besprochen werden sollte.
Grundsätzlich gilt es immer, das Risiko einer Rezidivblutung abzuschätzen. Wenn die Blutungsquelle behoben wurde (z. B. nach einer suffizienten Versorgung eines Aneurysmas oder einer anderen Gefäßfehlbildung), erscheint eine Antikoagulationstherapie sicher. Besteht die Blutungsquelle fort, ist das Risiko einer erneuten Blutung weiterhin hoch. So wurde beispielsweise unter Cumarin-Behandlung nach Lobärhämatom auf Basis einer zerebralen Amyloidangiopathie innerhalb eines Jahres bei 11 bis 15% der Patienten eine Rezidivblutung beobachtet.20 Somit ist das jährliche Blutungsrisiko in dieser Situation deutlich höher als das jährliche Risiko eines kardial-embolischen Schlaganfalls bei VHF – selbst bei hohem CHA2DS2-VASc-Score. Diese Daten stammen allerdings von einem Literaturreview aus dem Jahr 2003. Eine Metaanalyse von drei aktuelleren Observationsstudien weist dennoch auf den möglichen Nutzen einer Antikoagulation für Patienten nach einer lobären intrazerebralen Blutung hin.21 Diesbezüglich sind weitere Studien mit NOAKs geplant. Deutlich geringer war das Blutungsrisiko in einer Untersuchung aus dem Jahr 2003 bei einer Patientengruppe mit hypertensiven Stammganglien-ICHs (ca. 2% im ersten Jahr unter Cumarin-Behandlung). Damit erscheint in dieser Situation – vor allem, wenn der Blutdruck gut kontrolliert ist – eine Antikoagulationstherapie in der Nutzen-Risiko-Abwägung sinnvoll. Faktoren, die für oder gegen den Wiederbeginn einer Antikoagulation sprechen, sind in Tabelle 4 zusammengefasst.1
Wenn interdisziplinär die Entscheidung für eine Antikoagulationsbehandlung gefallen ist, sollte diese erst vier bis acht Wochen nach dem Akutereignis begonnen werden. Diese Empfehlung der Europäischen Kardiologischen Gesellschaft wird auch von einer aktuellen Analyse schwedischer Registerdaten unterstützt.1, 22

Antagonisierung der NOAK-Wirkung
Für Dabigatran steht mit Idarucizumab ein spezifisches Antidot zur Verfügung, ein monoklonaler Antikörper, der durch Bindung an Dabigatran dessen Wirkung antagonisiert.23
Seit April 2019 ist in der EU mit Andexanet alfa auch ein Antagonist für Rivaroxaban und Apixaban zugelassen (in Deutschland verfügbar seit September 2019). Hierbei handelt es sich um einen rekombinanten Faktor Xa, der mit dem körpereigenen Xa um die Bindung des NOAK konkurriert. Sehr hohe Kosten und begrenzte Verfügbarkeit limitieren bisher den Einsatz. Die Zulassung erstreckt sich nicht auf Edoxaban, da hierfür keine Studiendaten erhoben wurden.
Im November 2020 wies die Europäische Arzneimittelbehörde darauf hin, dass Andexanet alfa nicht vor einer geplanten Heparinisierung eingesetzt werden solle, da die Substanz die gerinnungshemmende Wirkung von Heparin beeinträchtige.
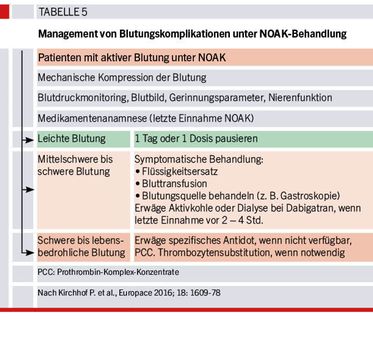
Management von Blutungskomplikationen unter NOAK-Therapie
Bei Patienten mit Blutungen unter NOAK-Behandlung sind zunächst Allgemeinmaßnahmen wie mechanische Kompression der Blutung, Monitoring der Vitalparameter sowie eine akute Laborabklärung indiziert. Ferner sollte – sofern möglich – die Medikamentenanamnese (welche Substanz, welche Dosis, wann zuletzt eingenommen) erhoben werden. Da die Behandlungsentscheidung aufgrund der klinischen Präsentation und des Schweregrades der Blutung erfolgt, sind die spezifischen Gerinnungstests für die einzelnen Substanzen nicht unbedingt notwendig.
Bei leichten Blutungen kann die NOAK-Behandlung einfach für eine Dosis oder einen Tag pausiert werden. Mittlere bis schwere Blutungen machen häufig zusätzlich Bluttransfusionen bzw. Flüssigkeitsersatz notwendig oder bedürfen einer operativen Versorgung der Blutungsquelle. Wurde Dabigatran in den letzten zwei bis vier Stunden eingenommen, kann die Gabe von Aktivkohle oder die Durchführung einer Dialyse erwogen werden (die anderen NOAKs sind nicht dialysierbar). Bei schweren und lebensbedrohlichen Blutungen sollte ein spezifisches Antidot gegeben werden. Ob Prothrombin-Komplex-Konzentrate zur Reversierung des antikoagulatorischen Effekts bei NOAKs effizient sind, ist noch unklar. Von den meisten Fachgesellschaften wird ein Behandlungsversuch in einer Dosis von 2.000IU bzw. 1.500IU (< 65 kg KG) bei schweren, lebensbedrohlichen Blutungen empfohlen (Tab. 5).
Operationen unter laufender NOAK-Behandlung
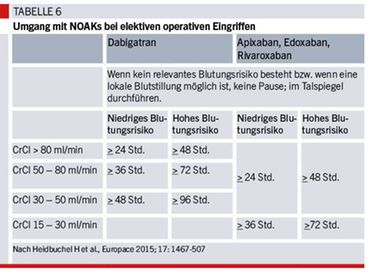
Wie lange und ob überhaupt die NOAK-Behandlung pausiert werden muss, hängt vom Blutungsrisiko der Operation ab. Eingriffe ohne relevantes Blutungsrisiko bzw. wenn eine lokale Blutstillung problemlos möglich ist, sollten im Talspiegel des NOAK durchgeführt werden (nach 12 Stunden bei zweimal bzw. nach 24 Stunden bei einmal täglicher Einnahme). Aufgrund der ähnlichen Plasmahalbwertszeiten aller NOAKs erscheint es im Zweifelsfall sinnvoll, bei zweimal täglicher Einnahme eine Dosis auszulassen und etwa sechs Stunden nach dem Eingriff wieder mit einem NOAK zu beginnen. NOAKs sollten bei Eingriffen mit niedrigem Blutungsrisiko auf alle Fälle für 24 Stunden und bei hohem Blutungsrisiko für 48 Stunden pausiert werden. Diese Zeit verlängert sich in Abhängigkeit von Substanz und Nierenfunktion auf bis zu 96 Stunden bei Dabigatran (Tab.6).5 Eine Umstellung von NOAK auf Heparin in der Übergangsphase („Bridging“) ist nicht indiziert und geht mit einem erhöhten Blutungsrisiko einher.
Beispiele für Eingriffe, die unter laufender NOAK-Behandlung erfolgen können, sind Extraktion von ein bis drei Zähnen, Kataraktoperationen oder auch kleinere dermatologische Exzisionen. Ein niedriges Blutungsrisiko besteht beispielsweise bei Endoskopien mit Biopsie, Prostatabiopsie oder Schrittmacherimplantation, während bei Lumbalpunktion, Epiduralanästhesie, Thorax- oder Bauchoperationen, Nierenbiopsie oder transurethraler Prostataresektion ein hohes Blutungsrisiko anzunehmen ist (vollständige Liste siehe5). Im Endeffekt ist jedoch die Entscheidung, wie lange bei welchem Eingriff die Antikoagulationstherapie pausiert wird, individuell zu stellen.
Thrombolysebehandlung unter laufender AK-Therapie
Eine bestehende orale Antikoagulation ist laut Zulassung von Alteplase in Europa eine Kontraindikation, sodass eine intravenöse Lysetherapie bei akutem Schlaganfall in dieser Konstellation immer einen individuellen Heilversuch (Off-Label-Behandlung) darstellt. Im Fall von Cumarinen kann bei einem INR-Wert ≤ 1,7 unter sorgfältiger Nutzen-Risiko-Abwägung mit Alteplase behandelt werden. Bei Patienten unter laufender NOAK-Behandlung kann eine systemische Lysetherapie erwogen werden, wenn keine wirksame Antikoagulation zum Zeitpunkt der Verabreichung besteht. Dies ist gegeben, wenn in den letzten 48 Stunden kein NOAK eingenommen wurde und die Nierenfunktion sowie die globalen Gerinnungswerte normal sind. Alternativ kann durch spezifische Gerinnungstests der einzelnen Substanzen eine antikoagulatorische Aktivität vor Verabreichung einer Lysetherapie ausgeschlossen werden (vgl. etwa das Positionspapier der Österreichischen Schlaganfallgesellschaft 2017; www.oegsf.at).
Aufgrund der raschen und kompletten Aufhebung der Wirkung von Dabigatran durch Idarucizumab wurden weltweit bereits mehrere Patienten nach Antagonisierung mit einer i.v. Lysetherapie behandelt.23 Es bedarf jedoch noch mehr Erfahrung, um Effizienz und Komplikationen dieses Vorgehens zu bewerten.
Sonderfall ESUS?
Bei Langzeit-EKG-Ableitungen von Patienten mit unklarer Schlaganfallursache konnte in bis zu 30% der Fälle (z. B. CRYSTAL-AF-Studie mit implantierbarem Loop-Rekorder über drei Jahre) ein intermittierendes Vorhofflimmern nachgewiesen werden.24 Aufgrund des besseren Sicherheitsprofils von NOAKs gegenüber den Cumarinen stellt sich die Frage, ob die Gruppe der Patienten mit nicht offensichtlicher Schlaganfallursache nicht auch von einer NOAK-Gabe profitieren würde. Dazu wurde der Begriff des ESUS („embolic stroke of undetermined source“ – embolischer Schlaganfall von unklarer Quelle) geschaffen, er bezeichnet einen nichtlakunären Schlaganfall ohne höhergradige Gefäßstenose (<50%), ohne kardiale Emboliequelle und ohne andere bekannte Ursache, z. B. Vaskulitis, Migräne oder Drogenmissbrauch.25 Eine Studie mit Rivaroxaban gegen Aspirin in dieser Patientengruppe wurde nach einer Zwischenanalyse vorzeitig abgebrochen, da Rivaroxaban keinen Vorteil in der Sekundärprävention des Schlaganfalls erbrachte. Die Daten wurden zwischenzeitlich publiziert.26 Hier fällt auf, dass im Aspirin-Arm eine überraschend geringe Blutungsrate aufgetreten ist. In der korrespondierenden Studie mit Dabigatran konnte auch keine Überlegenheit der NOAK-Behandlung gegenüber Aspirin gefunden werden.27 Die Rate an schweren Blutungen war in der Dabigatran-Gruppe nicht erhöht, sehr wohl aber die Anzahl der nicht schweren, jedoch klinisch relevanten Blutungen. Eine Studie mit Apixaban mit strengeren Einschlusskriterien läuft noch. Derzeit ist die Behandlung von Schlaganfallpatienten ohne Vorhofflimmern mit NOAKs eine Off-Label-Therapie.
Fragen zur zertifizierten Fortbildung: „NOAKs als Sekundärprophylaxe bei Schlaganfall“
Frage 1
Für welche Indikation sind nicht-Vitamin-K-abhängige orale Antikoagulanzien (NOAKs) nicht zugelassen?
a) Primär- und Sekundärprävention von Schlaganfällen bei mechanischen Herzklappen
b) Primär- und Sekundärprävention von Schlaganfällen bei Vorhofflimmern
c) Sekundärprävention der tiefen Venenthrombose
d) Sekundärprävention der Lungenembolie
e) Prophylaxe von venösen Thromboembolien bei elektivem Hüft- oder Kniegelenkersatz
Frage 2
Welche der folgenden Aussagen über die Behandlung mit NOAKs bei einem operativen Eingriff ist nicht richtig?
a) NOAKs müssen 1 bis 4 Tage vor einer geplanten Operation pausiert werden.
b) Bei Extraktion eines Zahnes müssen NOAKs nicht unbedingt pausiert werden.
c) Die Lumbalpunktion stellt einen Eingriff mit hohem Blutungsrisiko dar.
d) Die Dauer der Unterbrechung der NOAK-Behandlung vor einer Operation richtet sich nach den Nierenwerten, dem Blutungsrisiko des Eingriffs und der Art des NOAK.
e) Während der Behandlungspause von NOAKs sollte bis zum Vorabend der Operation niedermolekulares Heparin gegeben werden.
Frage 3
Welche Aussage über die Behandlung mit NOAKs trifft nicht zu?
a) Eine Sturzneigung stellt keine absolute Kontraindikation für die Behandlung mit einer oralen Antikoagulation dar.
b) Bei Patienten mit einem niedrigen CHA2DS2-VASc-Score soll Acetylsalicylsäure statt eines NOAK verabreicht werden.
c) NOAKs weisen das gleiche extrazerebrale Blutungsrisiko wie Cumarine auf.
d) Bei einer reduzierten Nierenfunktion mit einer Kreatinin-Clearance von 40 ml/min sollen die Nierenwerte alle vier Monate kontrolliert werden.
e) Bei der Verschreibung von NOAKs ist eine ausführliche Aufklärung des Patienten über die Substanz und mögliche Komplikationen notwendig.
Frage 4
Beginn einer oralen Antikoagulation nach ischämischem Schlaganfall: Welche Aussage ist nicht richtig?
a) Nach einer TIA unter laufender NOAK-Behandlung kann diese fortgeführt werden.
b) Nach einer TIA kann am Folgetag mit einem NOAK begonnen werden.
c) Für den frühen Beginn einer oralen Antikoagulation nach Schlaganfall spricht eine kleine Infarktgröße.
d) Bei einer jungen Patientin/einem jungen Patienten mit schwerem Schlaganfall bei Vorhofflimmern kann nach Ausschluss einer hämorrhagischen Transformation 12 Tage nach dem Ereignis mit einer Antikoagulation begonnen werden.
e) Nach einem Schlaganfall kann früh mit einer reduzierten Dosis der NOAKs begonnen werden.
Frage 5
Welche der folgenden Aussagen über das Management von Patienten unter NOAK-Behandlung trifft nicht zu?
a) Eine suffiziente orale Antikoagulation stellt eine Kontraindikation für eine intravenöse Lysetherapie dar.
b) In Abhängigkeit von den spezifischen Gerinnungstests der NOAKs kann bei mittelschweren Blutungen auf eine Antagonisierung verzichtet werden.
c) Idarucizumab stellt ein effizientes spezifisches Antidot für Dabigatran dar.
d) Eine Spiegelbestimmung unter Leitliniengerechter NOAK-Behandlung ist nicht notwendig.
e) Eine intrazerebrale Blutung unter laufender NOAK-Behandlung ist langfristig eine Kontraindikation für eine orale Antikoagulation.
Frage 6
Welches der folgenden Medikamente sollte nicht oder nur mit Vorsicht mit einem NOAK kombiniert werden?
a) Ketoconazol
b) Pantoprazol
c) Citalopram
d) Atorvastatin
e) Digoxin
Frage 7
Eine reduzierte Dosis von Apixaban (2x 2,5mg) soll in der Schlaganfallprophylaxe bei Vorhofflimmern eingesetzt werden bei:
a) Alter > 70 Jahre und Körpergewicht < 60kg
b) Alter > 80 Jahre
c) vermehrter Sturzneigung
d) Alter >70 Jahre und Serumkreatinin ≥1,5mg/dl
e) Alter >80 Jahre und Serumkreatinin ≥1,5mg/dl
Frage 8
Bei korrekter Anwendung des CHA2DS2VASc-Scores gilt:
a) Ab einem Score von 1 Punkt ist immer eine Antikoagulation indiziert.
b) Bei Personen <65 Jahre mit Vorhofflimmern ohne weitere Risikofaktoren ist das Schlaganfallrisiko sehr niedrig.
c) Patienten <65 Jahre benötigen nach einer TIA keine Antikoagulation.
d) Patienten mit einem Score <2 sollen mit ASS behandelt werden.
e) In der Bewertung werden Hypertonie, Diabetes mellitus und Hypercholesterinämie berücksichtigt.
Frage 9
Welche Aussage ist richtig? Für alle NOAK-Dosierungen gilt im Vergleich zu Cumarinen:
a) Sie reduzieren das Schlaganfallrisiko wirksamer als Cumarine.
b) Sie haben ein niedrigeres generelles Blutungsrisiko.
c) Sie benötigen seltenere Spiegelbestimmungen.
d) Die Wirkung setzt wenige Stunden nach der ersten Einnahme ein.
e) Sie erfordern eine überlappende Heparingabe.
Frage 10
Dabigatran unterscheidet sich von den anderen NOAKs in einigen Punkten. Welche Antwort trifft zu?
a) Dabigatran wird einmal täglich eingenommen.
b) Dabigatran muss einschleichend dosiert werden.
c) Es wird eine Dosisreduktion für Patienten >80 Jahre empfohlen.
d) Der Therapieeffekt muss durch INR-Kontrollen kontrolliert werden.
e) Andexanet alfa ist ein spezifischer Antagonist.